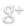Si queremos realizar la estructura de Lewis del amoníaco (NH3) seguiremos lo siguientes pasos.
Comience por dibujar la estructura general de la molécula uniendo los átomos de hidrógeno con el nitrógeno con enlaces simples:
Ahora procederemos a contar los electrones de valencia totales de los átomos de hidrógeno (n H,val = 1) y nitrógeno (n N,val = 5), donde “n” sería la valencia del átomo:
3 H Valencia + N Valencia = 3 x 1 + 5 = 8
Luego tenemos que calcular el número de electrones necesarios para llenar completamente las capas de valencia para el hidrógeno y el nitrógeno.
El hidrógeno para completar su capa de valencia y por lo tanto, cumplir con la regla del octeto, necesita 2 electrones en su último orbital. Pero, como son tres átomos de hidrógeno, multiplicaremos estos dos electrones por tres.
Por otra parte, el nitrógeno para cumplir con la regla del octeto necesita 8 electrones en el último orbital.
Ahora realizamos la suma:
3 H última capa + N última capa = 3 x 2 + 8 = 14
El siguiente paso será restar los dos resultados que obtuvimos y así obtener el número de electrones enlazantes.
14 – 8 = 6 electrones enlazantes (tres enlaces).
Ahora si nos fijamos en el diagrama de lewis del amoniaco, veremos que ya tenemos esos 6 electrones (tres enlaces), por lo tanto ya tiene todos los enlaces necesarios.
Hay 3 enlaces y por lo tanto 6 electrones enlazantes en el diagrama.
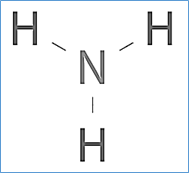
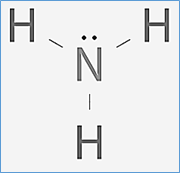
Por último, rellene los electrones no unidos que quedan en cada átomo. En total, quedan 8-6= 2 electrones, estos electrones los agregaremos al nitrógeno.
De esta manera obtendremos finalmente la estructura de lewis del amoníaco.