Ley de Boyle - Graficas - Formulas - Ejercicios Resueltos - Ejemplos

La Ley de Boyle enuncia que para una cantidad fija de gas a temperatura constante, la presión del gas es inversamente proporcional al volumen que ocupa.
Fórmula de la Ley de Boyle
La explicación de la Ley de Boyle se puede ver continuación:
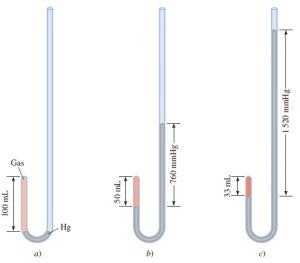
- Figura a - En primer lugar la presión ejercida sobre el gas es igual a la presión atmosférica y el volumen
del gas es de 100 mL. - Figura b - se ha añadido más mercurio a fin de duplicar la presión sobre el gas, con lo que el volumen del gas disminuye a 50 mL.
- Figura c - Se triplico la presión sobre el gas por lo tanto su volumen disminuye a un tercio de su valor inicial.
Lo anteriormente mencionado quedaria expresado matematicamente de la siguiente forma..
El símbolo ∝ significa proporcional. La formula se lee "La presion (P) es inversamente proporcional al volumen (V)".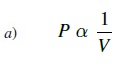
Se puede cambiar ∝ por el signo de igualdad y escribir la formula de la siguiente manera
K1 es una constante llamada constante de proporcionalidad. Esta formula (figura c) establece que el producto de la presión por el volumen de un gas a temperatura y cantidad de gas constantes es una constante.
Finalmente mediante estas acotaciones podremos obtener la expresión relacionada para dos gases, la cual se usaremos en varios de los ejercicios y problemas de gases ideales.
Pinicial Vinicial = Pfinal Vfinal
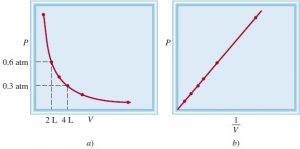
Gráficas basadas en la Ley de Boyle
- Gráfica (a) - Presión en función del volumen; P.V = K1 Corresponde a una hipérbola equilátera.
- Gráfica (b) - Presión en función de 1/V ; P = K1 . 1/V Corresponde a una función lineal.
Como resolver ejercicios y problemas de la Ley de Boyle - Mariotte?
Lo primero que te recomendaría es leer varias veces los ejercicios y tratar de anotar los datos del problema.
Una vez anotados los datos, tienes que tener en cuenta cual es el estado inicial y final del gas. Por lo tanto los datos del estado inicial los separaremos de los del estado final.
Siempre en este tipo de ejercicios nos van a dar solamente tres datos, el cuarto dato seria la incógnita ( solución a la respuesta).
Ejercicios para resolver aplicando la Ley de Boyle:
Pinicial Vinicial = Pfinal Vfinal (ECUACIÓN DE LEY DE BOYLE A UTILIZAR)
1) En un recipiente cerrado de 4 Litros se introduce Oxigeno hasta que este ejerce una Presión de 2 Atmósferas. Calcular la Presión que ejercerá el gas si reducimos el volumen hasta 2 Litros.
2) Tenemos Nitrógeno gaseoso en un recipiente de 0,8 Litros, ejerciendo una presión de 1,23 Atmósferas. ¿Cual es la nuevo volumen si aumentamos la presión del gas hasta 2 Atmósferas?.
3) La presión del Nitrógeno gaseoso en un tanque de 12 Litros es de 15,65 atmósferas a 27 ºC. ¿Qué volumen ocupara el gas a 4,0 atmósferas , si la temperatura permanece constante ?
4) Una muestra de Cloro gaseoso ejerce una presión de 3 Atmósferas. Finalmente se incrementó la presión a 3,6 Atmósferas, reduciendo el volumen hasta 1,6 Litros. ¿Que volumen inicial posee la muestra de Cloro?
Ejercicios resueltos de la Ley de Boyle
Problema 1
Una muestra de nitrógeno ocupa un volumen de 3,8 litros a una presión de 1,3 Atmósferas. ¿Cuál será el volumen de nitrógeno ocupado a una presión de 1 Atmósferas?. La temperatura permanece constante
Solucion: Anotaremos los datos que nos da el problema.
V1 = 3,8 Litros
P1 = 1,3 Atm
V2 = x
P2 = 1 Atm
Vemos que tenemos todos los datos, pero nos falta el V2 . Por lo tanto escribimos la ecuacion y despejamos.
Problema 2
Un globo contiene un gas que ocupa 2,31 litros a una presión de 2 atm. Si la temperatura a la que se encuentra permanece constante. ¿Que presion ejercera el gas en el globo si se lleva al volumen de 4 litros?.
Solucion: Anotaremos los datos que nos da el problema.
V1 = 2,31 Litros
P1 = 2 Atm
V2 = 4 Litros
P2 = x
Vemos que tenemos todos los datos, pero nos falta el P2 . Por lo tanto escribimos la ecuacion y despejamos.
Problema 3
El gas helio se mantiene en un depósito de 5 litros a 768 mm de Hg. El gas se contrae hasta un volumen de 3,4 Litros. Asumiendo que la temperatura permanece constante ¿Cuál sera la presión final que ejerce el gas?.
Solucion: Anotaremos los datos que nos da el problema.
V1 = 5 Litros
P1 = 768 mm de Hg
V2 = 3,4 Litros
P2 = x
Vemos que tenemos todos los datos, pero nos falta el P2 . Por lo tanto escribimos la ecuacion y despejamos.
Reemplazando los valores obtenemos el resultado final:
NOTA IMPORTANTE
Como se puede observar, siempre vamos a utilizar la misma ecuación para resolver los ejercicios de la ley de boyle.
Pinicial Vinicial = Pfinal Vfinal
¿Quién fue Robert Boyle?
Fue un Físico-Químico considerado como uno de los padres de la química moderna. Reconocido principalmente por su contribución a la ciencia con la famosa Ley de Boyle. Nació en Irlanda en la ciudad de Waterford el 25 de enero en el año 1627. Falleció en Inglaterra ciudad de Londres un 31 de diciembre del año 1691.
Robert Boyle analizó la relación que existe entre la presión y el volumen de una muestra de un gas. El observo que a una temperatura constante y cantidad determinada de gas a medida que la presión (P) aumenta, el volumen (V) disminuye. Así que para demostrar esto realizó un experiencia científica.
FUENTE: Robert Boyle - Wikipedia
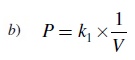
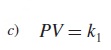
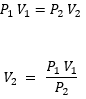
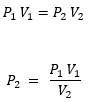

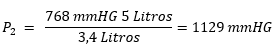

Deja una respuesta