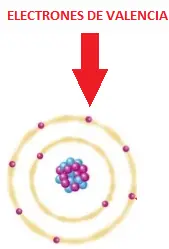
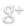Los electrones de valencia son los electrones ubicados en la capa más externa de un átomo.
¿Por qué estos electrones son especiales?
Son especiales ya que estos electrones son los primeros en participar en la reacción cuando dos átomos interactúan, son los más expuestos de todos lo electrones, por lo tanto, tienen una influencia esencial en las reacciones.
Tabla de Contenidos
¿Qué son los electrones de valencia?
Electrones de Valencia definicion: Son los electrones que se encuentran en la última capa electrónica (denominada orbitales de valencia) y tienen muchas posibilidades de participar en una reacción química. Estos electrones poseen el número cuántico principal n más alto.
Tienen vital importancia en la formación de moléculas y compuestos ya que determinan la capacidad del átomo para formar enlaces. Cuando un elemento se une a otro lo hace a través de sus electrones de valencia.
También se puede decir que estos electrones son los electrones más alejados al núcleo del átomo, y en consecuencia los que pueden participar comúnmente en la formación de enlaces químicos.
Se pueden representar fácilmente con estructuras de lewis. Por ejemplo, para la formación de la molécula de H2.
Orbitales de Valencia o Capa de Valencia
Es el lugar donde se encuentran ubicados los electrones de valencia, corresponde al último nivel del átomo. O más bien lo que sería el orbital más lejano.
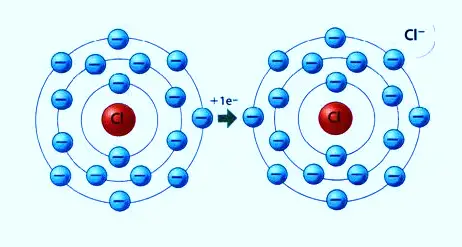
En esta imagen se puede apreciar claramente cuales son los electrones de valencia.
Propiedades y características según los electrones de valencia
Como mencionamos atrás, estos electrones de valencia son determinantes en la reactividad de un elemento, ya que determinan la facilidad con la que los elementos se unen a otros para formar un nuevo compuesto en cuestión.
Si observamos la capa de valencia de un gas noble, veremos que se encuentra completamente llena, entonces, este átomo no tiende a ganar ni perder electrones. Por este motivo se dice que los gases nobles no reaccionan en condiciones normales,o sea son inertes.
Generalmente, los elementos en los Grupos 1, 2, y 13 a 17 tienden a reaccionar para obtener una configuración electrónica similar al del gas noble más cercano, cuya configuración electrónica es ns2 np6.
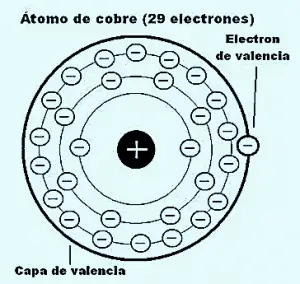
Por ejemplo los metales más reactivos, como lo son los del grupo 1 y 2 necesitan perder solo uno o dos electrones de valencia para formar cationes, y de esta manera obtener una configuración electrónica del gas noble más cercano.
Los no metales tienden a atraer electrones de valencia adicionales para formar enlaces iónicos o covalentes.
Los no metales más reactivos son los halógenos (elementos del grupo 17), como el Flúor y Cloro. Ambos tienen una configuración muy cercana a la del gas noble y necesitan únicamente un electrón de valencia para completar su octeto, por eso lo halógenos tienden aceptar dicho electrón proveniente de los metales alcalinos.
Dichos electrones de valencia participan en la conductividad eléctrica, por lo que un elemento se puede clasificar como metal, no metal o metaloide según su capacidad para conducir la electricidad.
Un metal sería un elemento que posee una alta conductividad eléctrica.
Un metaloide posee una conductividad eléctrica intermedia.
Un no metal posee nula conductividad.
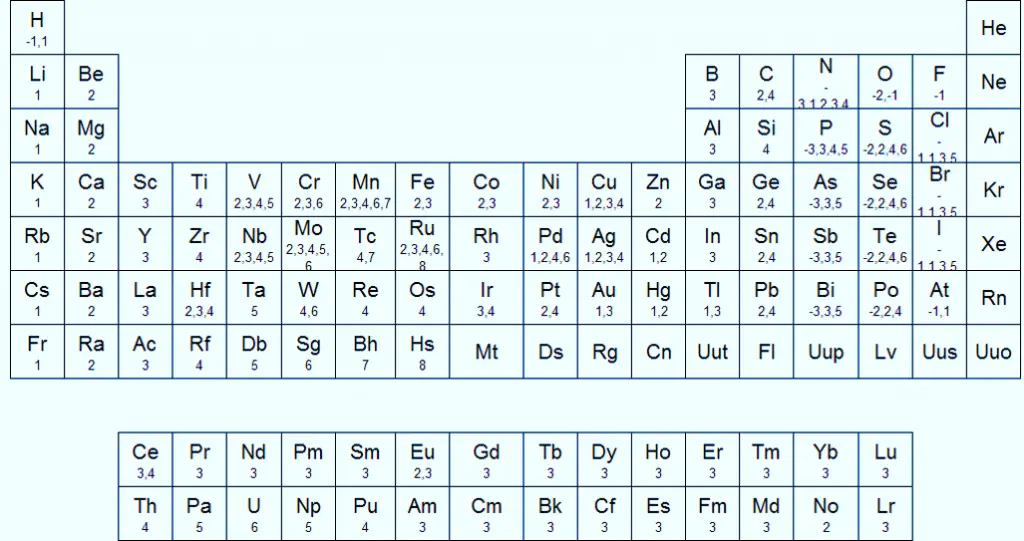
Tabla Periódica con valencias
En la tabla periódica los elementos se organizan según sus propiedades químicas y físicas de los elementos en función de su número atómico.
En la siguiente tabla se puede apreciar la valencia química de algunos elementos, no es necesario aprenderlos a todos. Solo los mas básicos, como la valencia del carbono, oxígeno, nitrógeno, azufre, boro, cloro, los del grupo uno y dos, ya que estos se utilizan normalmente como base de estudio para el Enlace Químico.
Hay dieciocho columnas verticales que se denominan Grupos y siete filas horizontales llamadas periodos.
Todos los elementos de un mismo grupo poseen el mismo número de electrones de valencia (Esto no ocurre en los metales de transición).
Los electrones de valencia aumentan en número a medida que se avanza en un período. Luego, al comenzar el nuevo período, el número disminuye a uno y comienza a aumentar de nuevo.
Por ejemplo, cuando en la tabla periódica se pasa del carbono al nitrógeno, y luego hacia el oxígeno, el número de electrones de valencia aumenta de 4 a 5 y luego a 6.
A medida que pasamos del flúor al neón y luego al sodio, el número de electrones de valencia aumenta de 7 a 8 y luego baja a 1 cuando comenzamos con el periodo del sodio.
Dentro de un grupo el número de valencia permanece igual (Esto no ocurre en los metales de transición).
Podemos determinar rápidamente el número de electrones de valencia que un átomo posee mirando la posición de su grupo en la tabla periódica.
Si prestamos atención a las valencias de la tablas periódica, En el grupo uno (el de los metales alcalinos) el número de valencia es 1.
Lo mismo sucede con el grupo dos (el de los metales alcalinotérreos) donde sus valencias es justamente 2.
Grupo en la tabla periódica | Electrones de valencia |
Grupo 1 (I) (Metales Alcalinos) | 1 |
Grupo 2 (II) (Metales Alcalinotérreos) | 2 |
Grupos del 3 al 12 (Metales de Transición) | **** |
Grupo 13 (III) (Grupo del Boro) | 3 |
| Grupo 14 (IV) (Grupo del Carbono) | 4 |
Grupo 15 (V) (Grupo del Nitrógeno) | 5 |
Grupo 16 (VI) (Grupo del Oxígeno) | 6 |
| Grupo 17 (VII) (Grupo de los Halógenos) | 7 |
| Grupo 18 (Gases Nobles) | 8 |
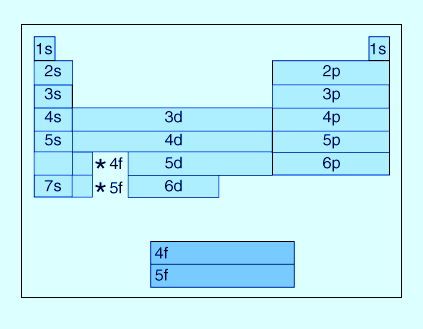
En los elementos del bloque s, y bloque p, el número de grupo es igual al número de valencia.
Algunas valencias de los elementos químicos
Número de valencia del carbono: 4
Número de valencia del Oxigeno: 6
Número de valencia del Nitrógeno: 5
Número de valencia del Azufre: 6
Número de valencia del Cloro: 7
Número de valencia del Fósforo: 5
NOTA: NO CONFUNDIR VALENCIA CON ESTADO DE OXIDACIÓN.
En otro curso se explicará la manera de saber la valencias de los demás elementos a partir de su configuración electrónica, con la cual también aprenderemos a denotar su estructura de lewis.
Bibliografía: Química general -Libro de Ralph H. Petrucci