Ley de Graham | Efusion y Difusion de Gases
Ley de graham
En el año 1932, el químico escocés Thomas Graham (1805-1869) Llevó a cabo una serie de experimentos sobre las velocidades de efusión de los gases.
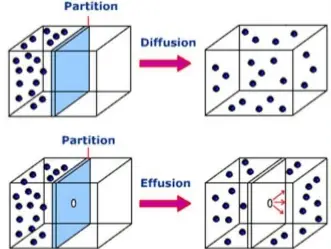
Se refiere a la velocidad con que distintos gases atraviesan por ejemplo, una pared porosa. Si la temperatura es constante la velocidad de efusión de un gas es inversamente proporcional a la raíz cuadrada de su masa molar.
La ley de Graham enuncia que la velocidad de efusión es inversamente proporcional a la densidad del gas según:
Para dos gases cualesquiera (siendo K la constante de proporcionalidad) :
Dividiendo ambas expresiones:
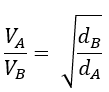 Graham dio con otra forma de calcular pesos moleculares de gases a partir de medidas experimentales. . Utilizando la ecuaciones de los gases ideales despejamos la densidad:
Graham dio con otra forma de calcular pesos moleculares de gases a partir de medidas experimentales. . Utilizando la ecuaciones de los gases ideales despejamos la densidad:
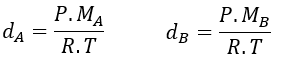 Reemplazamos la densidad de ambos gases en la ecuaciones de velocidad. Como la Presión P y la Temperatura T son constantes, simplificamos, y la ecuación de Graham queda de la siguiente manera:
Reemplazamos la densidad de ambos gases en la ecuaciones de velocidad. Como la Presión P y la Temperatura T son constantes, simplificamos, y la ecuación de Graham queda de la siguiente manera:
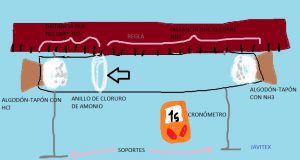
A cualquier temperatura y presión, la densidad y la masa molar de un gas son directamente proporcionales. Esto se puede comprobar con un experimento muy sencillo que consiste en colocar en un tubo de vidrio muy limpio, en forma simultánea dos tapones de algodón embebidos, uno con en solución de HCl (Ácido clorhídrico) y el otro en NH3 (Amoniaco). Al cabo de unos minutos se observa la formación de un anillo de humo blanco de NH4Cl (Cloruro de Amonio) como producto de la siguiente reacción.
HCl + NH3 ⇒ NH4Cl
La difusión de los gases
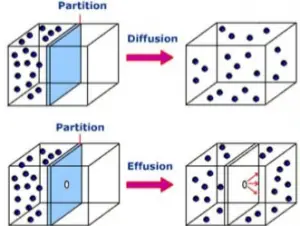
Es el fenómeno asociado al movimiento aleatorio de las moléculas de un gas que se mezcla con las moléculas de otro gas, en virtud de sus propiedades cinética. A pesar de que las velocidades moleculares son muy grandes, el proceso de difusión toma un tiempo suficientemente grande para completarse Esto se debe a que las moléculas experimentan numerosas colisiones mientras están en movimiento. Por ello la difusión de los gases sucede en forma gradual y no en forma instantánea.
La efusión de los gases
Es el pasaje del gas por un pequeño orificio hacia el vacío. Nos provee los datos que muestran como las velocidades de las moléculas del gas están relacionadas con la masa molar y la temperatura.
[pt_view id="28318365ro"]
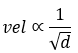
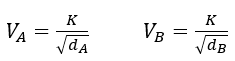
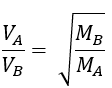
Deja una respuesta